遗传性视网膜疾病(IRD)是造成视觉障碍的300多种单基因原因的一组,全世界的患病率是1:1,000。目前仅可治疗一种IRD形式,但正在评估其余IRD的多种遗传疗法,其最终目的是改善视力,并在可接受的治疗干预次数和优化的患者负担下持久地改善视力。
基于此,Artur Cideciyan 等人再次在《Nature Medicine》发表题为:“Durable vision improvement after a single treatment with antisense oligonucleotide sepofarsen: a case report ”的临床实验论文,研究团队详细介绍了第11位患者,该患者仅接受了1次注射,在随后15个月的观察中,该患者的视力得到了持续改善。
提出了一种新的治疗方法,该方法使用AON来通过剪接调节来纠正常见的深度内含子突变。设计了10-体的17-mer 2'- O-甲基修饰的硫代磷酸酯RNA AON ,并进行了临床试验(NCT03140969)。根据源自正常动物和患者培养细胞的数据,该临床试验的给药方案是每3个月向玻璃体内重复注射Sepofarsen。前十名患者的初步结果提示疗效。参加试验的第11位也是最后一位患者,是内含子突变的纯合子,主观视觉改善,拒绝重复给药以避免潜在的透镜性不良事件;但是,继续监视是可以接受的。单一治疗的结果以及随后的15个月的仔细表型分析的详细信息提供了一个独特的机会来确定体内Sepofarsen功效的寿命和动力学。可以将P11的结果与其他5例患者进行比较,这些患者按照方案7接受了相同的初始剂量,并在3个月及以后的时间点接受了后续剂量。
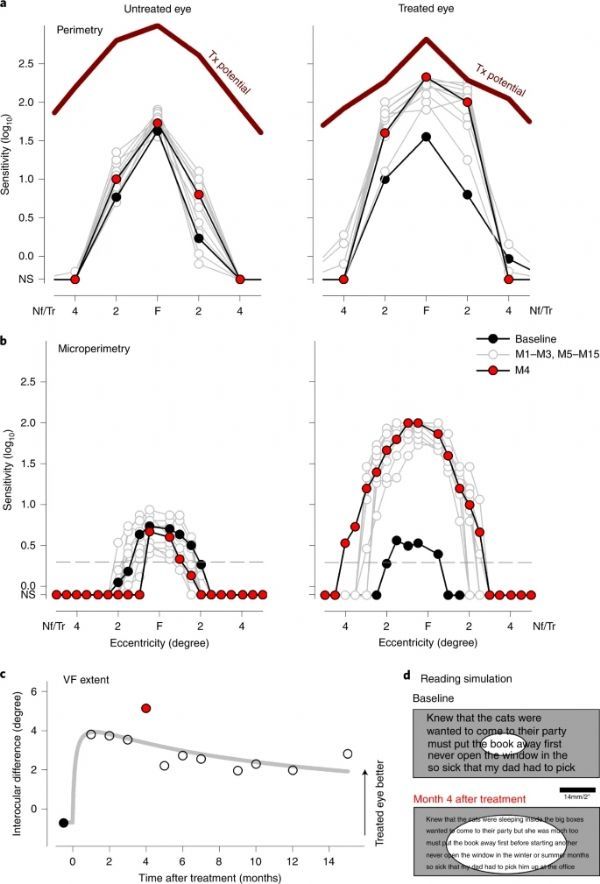
接下来,在P11中保留着动眼控制并伴有中心凹固定和小幅度眼球震颤,从而有机会评估光敏性的空间分布。使用自由视野视野检查法,仅在经过治疗的眼睛的中心4°范围内,灵敏度有了显着提高。根据视网膜结构的人工智能估计,中心凹和2°偏心位置几乎达到了其治疗潜力。为了更好地理解中央视野的变化,在较高的空间密度下进行了微视野测量,并实时跟踪和补偿了眼睛的运动。在接受治疗的眼睛中,整个中央视网膜的敏感性提高了超过1个对数单位。在治疗和未治疗的眼睛中,基线时视野的估计范围分别为2.6°和3.3°。治疗后四个月,视野范围在治疗的眼睛中扩大到7°,但在未治疗的眼睛中减小到1.8°。眼球视野差异在注射后1-4个月达到峰值。未经提示,报告治疗后阅读能力大大提高。在基线和第4个月测量的视敏度和视野范围的综合影响用于定量模拟,以解释阅读性能的可能变化。根据该模拟,与基线相比,预计治疗后患者将看到较小的字体和更多的单词。
最后,单次注射赛非森后,研究患者P11在所有记录的视觉功能和视网膜结构主观和客观测量中均表现出明显的时空一致性改善。功效在1个月时就可检测到,在3个月达到峰值,出乎意料的是,至少在15个月之前,所有功能指标均比治疗前更好。其发作和功效的峰值将预期取决于附加正常CEP290蛋白质合成由sepofarsen驱动,这估计要迅速吸收到兔光感受器和保持与2个月的半衰期动力学。一旦感光细胞中的Sepofarsen浓度下降并且新的CEP290合成停止,功效的长期持久性将由已经插入到纤毛过渡区的CEP290蛋白质的自然降解所决定。感光纤毛最大的隔室是OS,每隔10天进行翻新,显示出极高的营业额。
综上所述,通过使用反义寡核苷酸(AON)sepofarsen治疗,正在探索由于CEP290睫状体病导致的莱伯先天性黑桃病。一次玻璃体内注射Sepofarsen后,研究了一个较大队列的患者,进行了15个月的研究。注射后3个月左右,视觉功能和视网膜结构的相关测量值达到了实质性疗效峰值。在15个月时,即使有证据表明峰值反应减少,疗效仍然持续。功效动力学可以通过AON驱动的新的CEP290蛋白合成与人中央凹视锥细胞感光细胞中CEP290蛋白降解的自然缓慢速率之间的平衡来解释。










